更好的预测复发风险!III期结肠癌MRD队列研究成果发布
发布者:医学情报室 来源:医世象 2022-07-07
结直肠癌(CRC)是我国发病率和死亡率最高的癌症之一。手术切除仍是I-III期CRC最主要的治疗手段。但即使是根治性手术切除后,仍有30%-50%的肠癌患者会出现复发转移。 根治性手术联合辅助化疗是III期结肠癌患者的标准治疗策略。 根据目前的临床指南, 临床医生主要根据III期肠癌患者的临床复发风险来制定辅助化疗疗程,低危患者推荐进行3个月联合化疗,高危患者则推荐进行6个月的联合化疗。 因此,临床仍需要更精确的生物学标志物来指导III期结肠癌患者的个体化辅助治疗。
循环肿瘤DNA(ctDNA)是目前公认的检测术后微小残留病变(MRD)的有力工具。MRD与复发和预后密切相关。
共识分子分型(CMS分型)可反映肠癌本身内在的分子特征,CMS4型的结肠癌具有干性特征及间质型特征,生物学行为侵袭性强,且对治疗的敏感性差,预后较差。
为了证实将ctDNA与CMS分型联合是否能够对III期结肠癌患者进行更好的风险分层 ,复旦大学附属肿瘤医院大肠综合治疗科主任彭俊杰教授团队开展了一项前瞻性、观察性的单中心研究。该研究使用罗氏诊断CAPP-Seq液体活检产品对III期结肠癌患者术后MRD状态进行了评估。相关研究成果发表在European Journal of Cancer杂志(图1)[1]。
 图1. 彭俊杰教授团队在European Journal of Cancer杂志发表重要研究成果
图1. 彭俊杰教授团队在European Journal of Cancer杂志发表重要研究成果
该前 瞻性研究共纳入165例III期结肠癌患者,分别收集患者术后及化疗后的血浆。提取血浆ctDNA,使用ctDNA检测试剂盒进行197个癌症相关基因的DNA测序,同时收集患者的手术切除肿瘤组织进行788个基因的靶向RNA测序进行CMS分型。 在术后标本中,ctDNA的阳性率为15.9%;在化疗后标本中,ctDNA的阳性率为8.9%。 与ctDNA阴性患者相比, 术后ctDNA阳性患者复发风险增加3.6倍,化疗后ctDNA阳性患者复发风险增加3.3倍 (图2)。
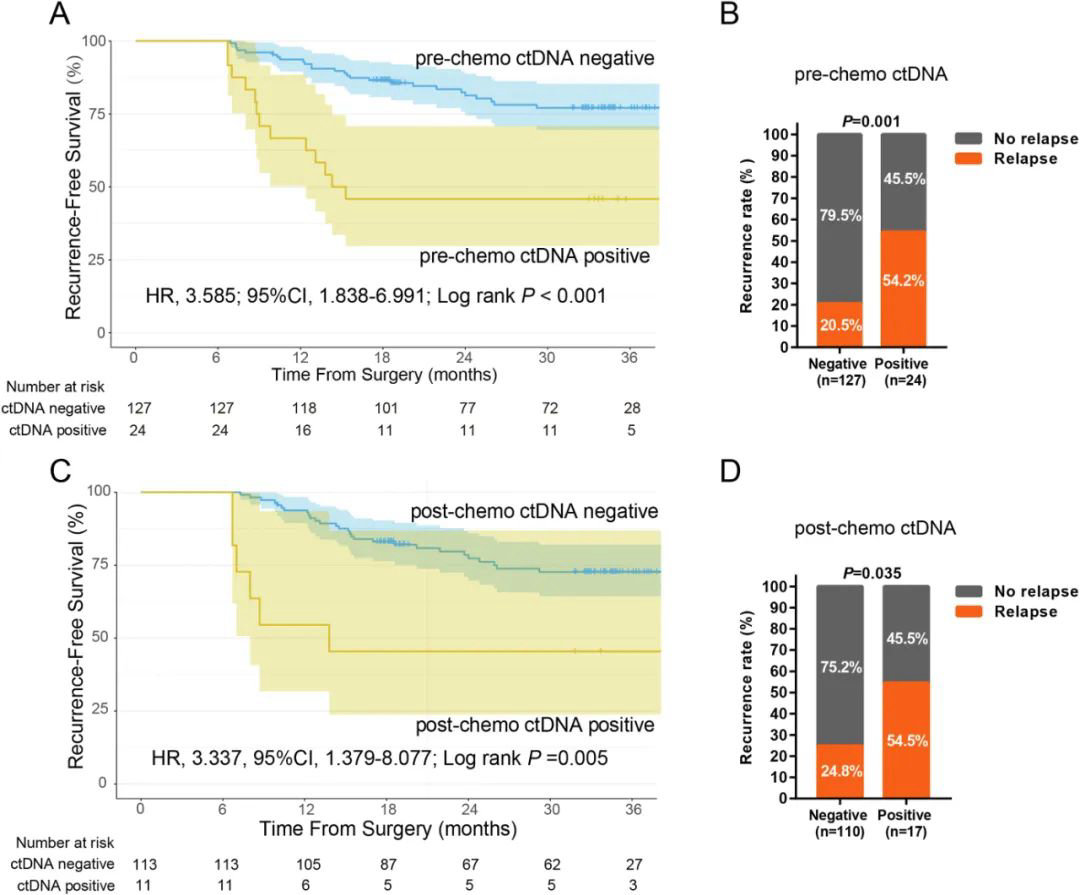 图2. 不同ctDNA状态的结肠癌患者无复发生存状态的生存曲线及对比情况
图2. 不同ctDNA状态的结肠癌患者无复发生存状态的生存曲线及对比情况
反映肿瘤本身生物学特性的CMS分型及临床复发风险分层均显示出了其预后预测能力(图3)。CMS4型结肠癌患者的复发风险是CMS1-3型患者的2.1倍;高危患者的复发风险是低危患者的3.3倍。
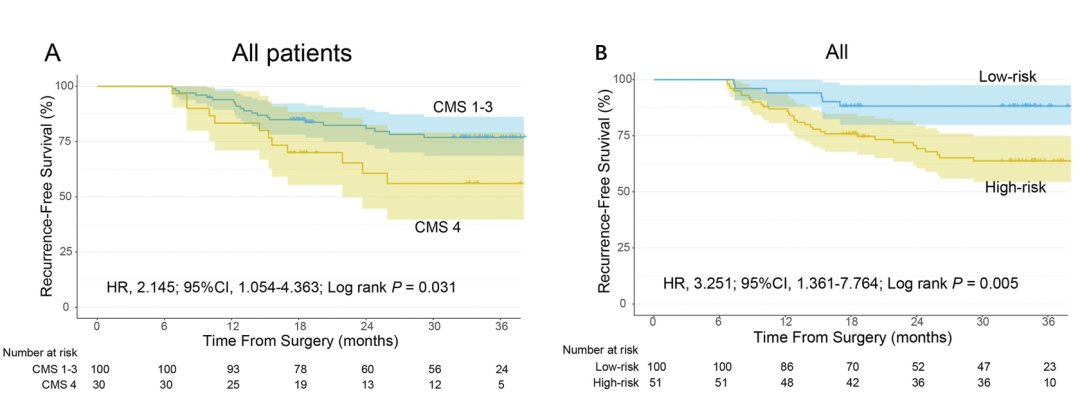
图3. 不同CMS分型及临床复发风险的结肠癌患者无复发生存状态的生存曲线。图片来源:Li Y, et al. , Eur J Cancer, 2022
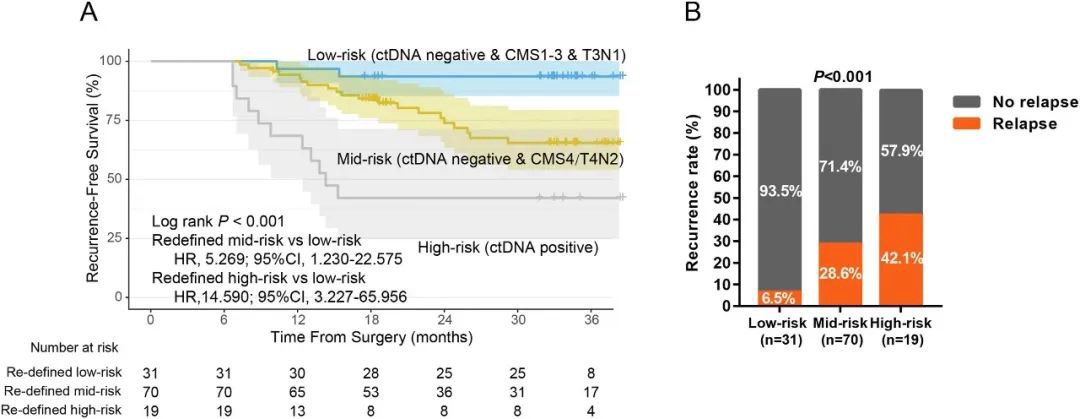
研究团队将ctDNA、CMS分型及临床风险结合,提出了新的III期结肠癌风险分层方法:
ctDNA阴性、CMS1-3型且病理分期为T3N1的患者为低危患者;
ctDNA阴性、CMS4型且病理分期为T4N2的患者为中危患者;
ctDNA阳性的患者为高危患者。
研究结果显示,III期结肠癌患者的复发风险可以通过新定义的风险分层标准进行有效分层(图4)。与重新定义的低危患者相比,中危患者的复发风险增加5.3倍,高危患者的复发风险增加14.6倍。
该研究证实 ctDNA可用于结肠癌术后复发风险的预测,术后ctDNA阳性患者的肿瘤复发风险显著增高 。 但是,在重视ctDNA检测对肿瘤预后预测价值的同时,也不能忽视肿瘤本身分子特性的重要性。 将ctDNA与CMS分型二者联合,能够更好地对肿瘤进行风险分层,从而指导个体化治疗。 研究团队提出,在重新定义的风险分层体系下,低危患者占所有患者的25.8%,该亚组的患者3年RFS高达93.5%,相当于I期结肠癌患者。该亚组患者是否仍需要辅助化疗,需要前瞻性、干预性临床试验的进一步证实。
同期相关研究突破
针对尚未明确的术后ctDNA检测是否可以应用于治疗决策使患者获益,Tie J等在《新英格兰医学杂志》(NEJM)上发表了关于ctDNA指导Ⅱ期结肠癌辅助治疗的临床试验 结果 [2] 。这是第一项公布的基于ctDNA的前瞻性、干预性肠癌术后辅助治疗随机对照 试验 [3] 。研究者对术后ctDNA阳性患者采取辅助治疗,对ctDNA阴性患者不采取辅助治疗。 结果表明,与传统临床病理特征指导的治疗方法相比, ctDNA指导下的辅助化疗策略能显著降低术后辅助治疗的使用,同时有着相似的无复发生存状态 。该项研究为术后ctDNA指导辅助治疗决策提供了直接的临床证据,为ctDNA指导的结肠癌术后精准诊治迈出了重要一步。
参考文献: [1] Li Y, Mo S, Zhang L, Ma X, Hu X, Huang D, et al. Postoperative circulating tumor DNA combined with consensus molecular subtypes can better predict outcomes in stage III colon cancers: A prospective cohort study, Eur J Cancer 2022;169: 198-209. [2] Tie J, et al. Circulating Tumor DNA Analysis Guiding Adjuvant Therapy in Stage II Colon Cancer. N Engl J Med. 2022. [3] 徐瑞华、王峰点评:NEJM发表ctDNA指导结肠癌辅助化疗
最新动态
- Cell:突破血脑屏障!张明君/王伊龙团队利用纳米颗粒“劫持”颅骨免疫细胞,让药物直达大脑,已开展人体临床试验 2026-01-22 14:56:22
- Adv Sci:上海交通大学王悍等团队发现增强前列腺癌放疗敏感性的潜在新策略 2026-01-22 14:55:23
- Nature:破解ALS自身免疫之谜——找到攻击神经元的“罪魁祸首”C9orf72蛋白,提供免疫治疗新路 2026-01-22 14:54:37
- Nat+Nat Med:破译脊髓损伤后血压紊乱的“神经密码”:揭示对抗性神经元结构,实现仿生电刺激精准双向调控 2026-01-22 14:53:44
- Nature:肠道菌群驱动T细胞可塑性,增强癌症免疫治疗效果 2026-01-22 14:52:51
- 早发糖尿病诊疗发现新依据 2026-01-22 14:51:42
- 肿瘤免疫抑制机制研究有新发现 2026-01-22 14:50:48
- 关节软骨损伤修复有新思路 2025-11-06 14:09:12
- 微型神经植入物可监测脑活动 2025-11-06 14:08:23
- Nature重磅:老药新用,逆转瘫痪!计算机虚拟筛选,发现脊髓损伤的再生疗法 2025-11-06 14:07:38